За сучасними уявленнями, атомне ядро складається з протонів і нейтронів, які є різними станами однієї частинки — нуклона. Загальне число нуклонів в атомному ядрі дорівнює цілочисловому, округленому значенню маси атомної А, яке називають числом масовим.
Загальна кількість нуклонів A, що входять до складу ядра, називається масовим числом ядра. Оскільки маса атома практично збігається з масою ядра, то масові числа ядер визначають і відносні атомні маси елементів, що також вказані в періодичній таблиці хімічних елементів. N = A – Z.
Встановлено, що число протонів в ядрі дорівнює порядковому номеру елемента в періодичній таблиці. Заряд ядра визначається числом протонів в ньому.
Загальні відомості Нуклонне число A можна знайти через визначення, A = Z + N, де Z є протонне число, а N — нейтронне число ядра. Для позначення нуклонного числа певного нукліда (атома), його можуть записувати: Або у вигляді верхнього індексу перед символом хімічного елемента (наприклад, 3He або 235U).
Завдання за темою з хімії
| Символ хімічного елемента | Порядковий номер елемента в періодичній системі | Кількість нейтронів у ядрі атома хімічного елемента |
|---|---|---|
| Mg | 12 | 24 – 12 = 12 |
Протон (p) — частинка, яка має заряд +1 і відносну масу, що дорівнює 1. Нейтрон (n) — частинка без заряду і відносною масою 1.
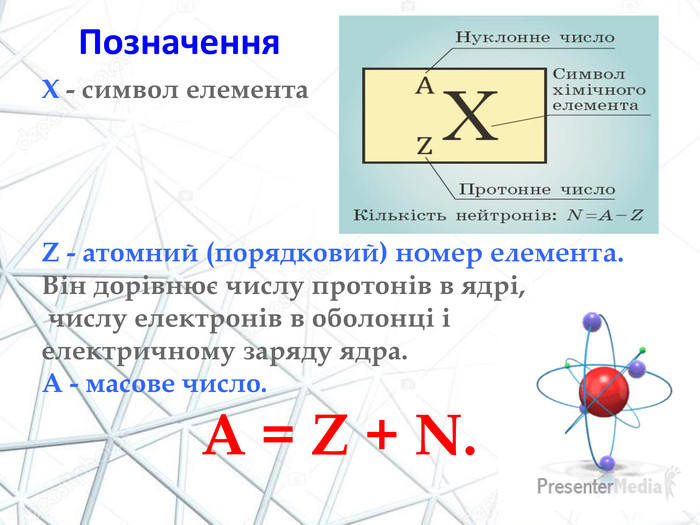

Повна кількість нуклонів у ядрі називається його масовим числом (зрозуміло, що = + та приблизно дорівнює середній масі атома, зазначеній у таблиці Менделєєва).