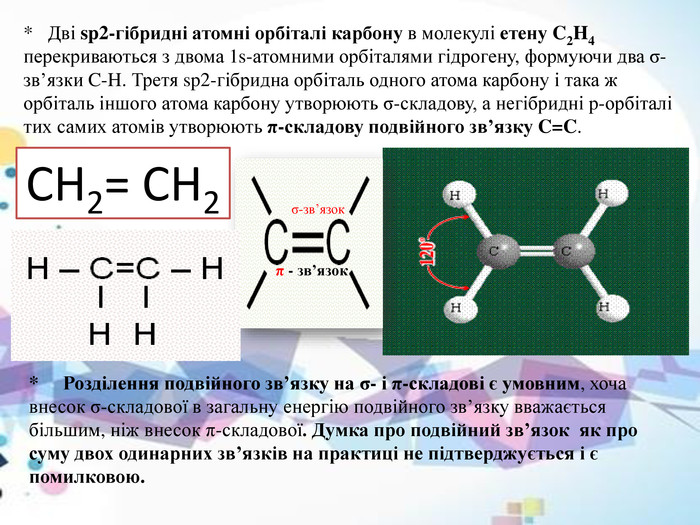
У молекулі етену між атомами Карбону — подвійний зв'язок (один — σ та один π зв'язок).
Хоча в молекулі етану є сім сигма-зв'язків, обертання близько шести вуглецево-водневих зв'язків не призводить до жодної зміни форми молекули, оскільки атоми водню по суті сферичні.
Так, у молекулі етану С2Н6 атоми Карбону сполучені одинарним зв'язком (С–С), в етені С2Н4 – подвійним (С=С), в етині С2Н2 – потрійним (С≡С). Одинарний зв'язок – це завжди σ-зв'язок, подвійний складається з σ + π-зв'язків, а потрійний – це сполучення σ + π + π-зв'язків (рис. 4.15).
Назва «етан» встановлена згідно з номенклатурою ІЮПАК. Префікс «ет-» посилається на присутність у карбоновому ланцюзі двох атомів вуглецю, а суфікс «-ан» — на присутність одинарного зв'язку між ними (тобто приналежність до алканів).
Сигма-зв'язок або σ-зв'язок — різновид ковалентного зв'язку, для якого характерна осьова симетрія. Сигма-зв'язки — найміцніші із ковалентних зв'язків.
При взаємодії атомів з однаковою електронегативністю утворяться молекули з ковалентним неполярним зв'язком.
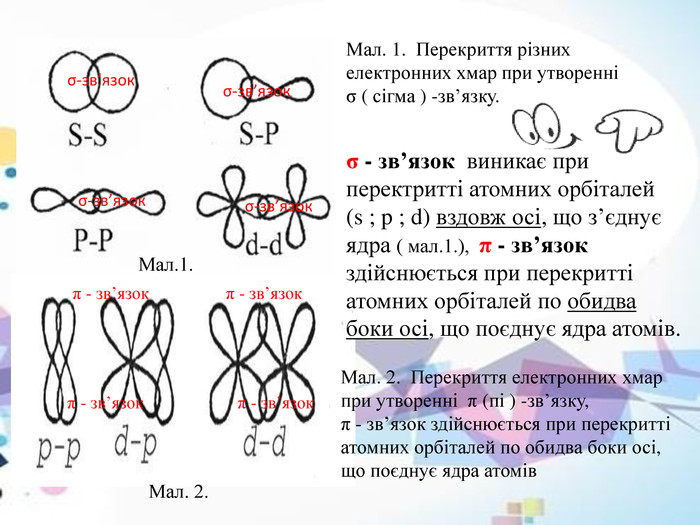
Сигма-зв’язок або σ-зв’язок — різновид ковалентного зв’язку, для якого характерна осьова симетрія. Сигма-зв’язки — найміцніші із ковалентних зв’язків.