4. Електронні формули. Електрони заповнюють енергетичні рівні в порядку послаблення притягання їх до ядра: спочатку s-, потім р-орбіталі, далі по одному, а якщо їх більше за число орбіталей, то по два, утворюючи електронні пари з протилежними спінами.
Енергетичні рівні складаються з підрівнів, причому номер рівня вказує на кількість підрівнів. Наприклад, у першого рівня є один підрівень, у другого — два підрівня, у третього — три і т. д. Енергетичні рівні нумерують, починаючи з найближчого до ядра.
Максимальна кількість електронів на третьому енергетичному рівні дорівнює 18, але у елементів третього періоду його заповнення не відбувається, тому що зовнішній електронний шар не може містити більше 8 електронів. На зовнішньому електронному шарі не може бути більше 8 електронів.
Число електронів на зовнішньому енергетичному рівні дорівнює номеру групи. На третьому енергетичному рівні крім s- та р-підрівні існує d- (максимально можливе число електронів – 10, енергетичних комірок – 5).
Кількість електронів на зовнішньому енергетичному рівні в атомі, визначають за номером групи (короткоперіодна форма періодичної системи), у якій розташований хімічний елемент у періодичній системі. Протонне число хімічного елемента дорівнює його порядковому номеру в періодичній системі.
І. Менделєєва містяться берилій Be , магній Mg , і 4 хімічних елемента, які називають лужноземельними: кальцій Ca , стронцій Sr , барій Ba , радій Ra . На зовнішньому енергетичному рівні атоми металів IIA групи мають два електрона. Тому для всіх лужноземельних металів характерна ступінь окиснення +2.

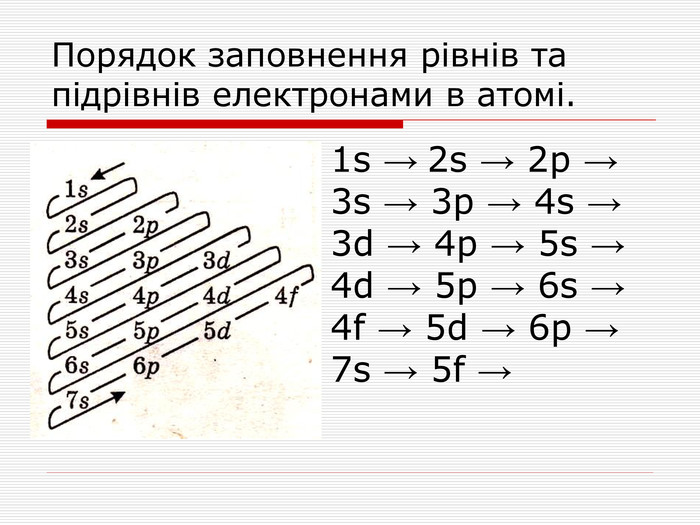
1. Заповнення електронних шарів атомів елементів малих періодів. Теорія: Загальна кількість електронів в атомі дорівнює порядковому номеру хімічного елемента в …